基于微流控的血細胞和干細胞流變學行為研究進展上
摘要: 微流控芯片作為一種微全分析技術平臺,具有精確流量控制、少量樣本需求和可集成化等諸多優勢,已被廣泛應用于生物醫學和環境科學等領域。利用微流控通道結構設計靈活的特點,可在實驗條件下模擬生理和病理條件下的復雜血管微環境,其與超分辨顯微成像技術的整合使得研究人員能夠實時觀察和分析微觀尺度下的細胞動態變化過程。因此,用微流控芯片系統研究細胞形態和力學特性方面也取得了重要進展。本文重點介紹了微流控芯片技術及基于微流控的數值仿真模擬手段在紅細胞、白細胞及干細胞變形和流變學行為中的應用及進展。首先,我們介紹了微流控芯片技術及相關數值仿真手段在紅細胞流動變形研究中的應用;接著,我們總結了微流控芯片系統及相關數值模擬在白細胞邊集及遷移行為的研究進展;此外,我們也概括了微流控芯片系統及相關數值模擬在干細胞遷移和定向分化機制方面的研究進展。最后,我們總結并展望了微流控芯片技術及其相關的數值模擬在血細胞及干細胞流變學研究中的挑戰和未來發展趨勢。
引 言
微流控芯片(Microfluidics)是一種集成了微流體技術和芯片制造技術的新型實驗平臺,用于控制微量液體和顆粒在微小尺度下的運動和反應。該技術通過微型化和集成化設計,實現了對微量液體及顆粒的高精度操控和實時監測,具有高通量、快速分析和低成本等優點,目前已廣泛應用于生物醫學和環境科學等研究領域。特別地,由于微流控芯片具有設計靈活的優勢,可通過各類通道及電子元器件的排列組合來模擬人體組織內的脈管系統,為細胞培養提供穩定的微環境。因此利用微流控芯片技術已經成為血細胞和干細胞變形和流動性研究的重要工具。此外,數值仿真技術與微流控芯片技術的結合可進一步幫助人們深入研究細胞行為。依托細胞幾何形態和力學特性,在細胞整體水平建立細胞數值仿真模型,可用于模擬研究細胞流變學行為、分析預測多種外部及內部因素對細胞流變學特性的影響規律,并對微流控芯片結構的優化設計提供一定的理論指導。
紅細胞(Red blood cell,RBC),又稱紅血球,呈雙凹盤狀,直徑約為 7-8 微米。紅細胞膜為薄的脂質雙層膜,內部充滿血紅蛋白溶液,屬于高度可變形的充液彈性薄殼體。紅細胞是血液中數量最多的一種血細胞(約占血液壓積的 45%),能隨血液流動遍及全身,負責運輸氧氣和二氧化碳,維護組織器官的正常功能。在血液循環過程中,紅細胞會穿過各種尺寸的血管,大到 4 毫米到小到 5 微米,承受著重力、拉力和剪切力。然而,在病理條件下,紅細胞的變形能力降低,血液的高切應力增加,會導致外周阻力增大,影響血液循環以及組織和器官的血液供應。因此,研究紅細胞在生理和病理條件下的變形性能對于理解血液循環及相關血液疾病的臨床表現具有重要意義。微流控通道可在實驗條件下模擬生理和病理條件下的復雜血管微環境,可用于探索紅細胞在毛細血管或多級血管分支網絡中的流動行為和變形性能,模擬體內微血管堵塞及血栓形成過程。在此基礎上,為了進一步量化分析紅細胞在微通道內的流變學行為,我們也對基于微流控芯片系統建立的相關數值仿真模型模擬研究進行了分析總結。
白細胞是一種無色有核的血細胞,體積比紅細胞大,一般情況下形狀接近球形,大小約為10-12 微米。白細胞具有活躍的活動能力,能夠從血管內遷移到血管外,或從外周組織遷移到血液循環中。因此,除了存在于血液和淋巴中,白細胞也廣泛分布于血管和淋巴管以外的組織中,在人體免疫系統中發揮著重要作用,包括對損傷或感染的炎癥區域作出反應。白細胞從血液到靶組織的外滲和遷移是炎癥反應的重要步驟。這個多步驟過程受到血流動力學和各種生化信號的嚴格調控。因此,白細胞外滲過多、時間過長或定向錯誤是動脈粥樣硬化、類風濕性關節炎、炎癥性腸病和多發性硬化等多種炎癥性疾病的發病機制之一。因此,借助微流控技術并結合數值仿真模擬研究白細胞遷移動力學過程具有非常重要的意義。
再生醫學和基于干細胞(Stem cell,SC)的細胞治療已成為當今世界各國先進生物醫療技術關注的焦點。其主要細胞來源是具有自我更新和多向分化潛能優點的干細胞。以被認為最接近臨床應用的干細胞產品——間充質干細胞(Mesenchymal stem cell,MSC)為例,許多臨床試驗已經研究了間充質干細胞在治療炎癥損傷組織、腦和脊髓損傷等疾病中的療效。干細胞療法產生療效的基礎是干細胞的歸巢行為(Homing),即在趨化因子的作用下從循環系統遷移到靶向部位的過程。隨后干細胞將進行定向分化,從而起到組織再生的治療作用。因此,基于干細胞的治療面臨的主要挑戰之一是如何提高細胞的歸巢效率。歸巢行為分為被動歸巢(堵塞在微血管中跨內皮遷移)和主動歸巢(主動貼壁后跨內皮遷移),它們不僅受遺傳和化學因素的影響,其力學表型也至關重要。細胞的硬度、膜張力和變形能力等力學特性會直接影響細胞在血管中的變形、流動和組織中的遷移等過程。傳統的細胞研究方法無法為異質性較高的干細胞提供足夠精準高效的力學表型數據,而微流控技術不僅成本低、通量高,還可模擬并調控干細胞生長、遷移分化所需的小生境(Niche)。因此,微流控芯片系統為觀察和調節干細胞的力學特性,并系統研究細胞歸巢、遷移和分化等功能提供了有力的工具。
隨著計算機技術的發展,數值仿真模擬技術也日漸成為血細胞和干細胞流變學行為研究中的重要工具之一。基于微流控芯片系統的數值仿真技術的可用于微流道結構優化設計、實驗參數敏感性分析等。基于彈性理論和流體力學的連續體力模型和基于粒子模擬方法的離散網格模型是目前研究血細胞流動和變形行為的兩大主流模型。連續體力模型(如浸入式邊界法和邊界積分法)是基于歐拉網格求解方法建立的,通常將細胞膜和細胞液視為均質材料,容易實現與現有的計算流體力學求解器耦合,常用于模擬含有大量血細胞的血液流動及細胞交互作用。基于粒子的離散網格模型(如多粒子碰撞動力學方法、光滑耗散粒子動力學方法和光滑粒子動力學方法)是將細胞膜、細胞液和血漿視為粗粒化粒子,其優勢主要體現在處理細胞膜復雜微結構問題上,如病理狀態下細胞膜與細胞骨架的分離現象、細胞膜的熱漲落等。需要注意的是,此方法在進行流體運動的模擬計算時,并非嚴格遵循納維-斯托克斯方程,導致該方法的計算精度較低。
本文綜述了近年來微流控芯片系統及基于微流控芯片的數值仿真模型模擬在血細胞和干細胞流變學行為中的研究進展(如圖 1)。本文首先介紹了微流控芯片技術及基于微流控系統的數值仿真技術在紅細胞變形研究中的應用;接著介紹了微流控芯片系統及相關數值模擬模型在白細胞邊集和遷移行為研究中的應用。在干細胞歸巢研究中,微流控芯片系統可以通過設計特定的微流道結構和生物信號化學梯度,模擬干細胞在體內歸巢的過程,研究干細胞遷移和定向分化的機制,并為干細胞治療提供指導。鑒于干細胞歸巢的數值模型仿真工作較少,只對其進行了簡要介紹。
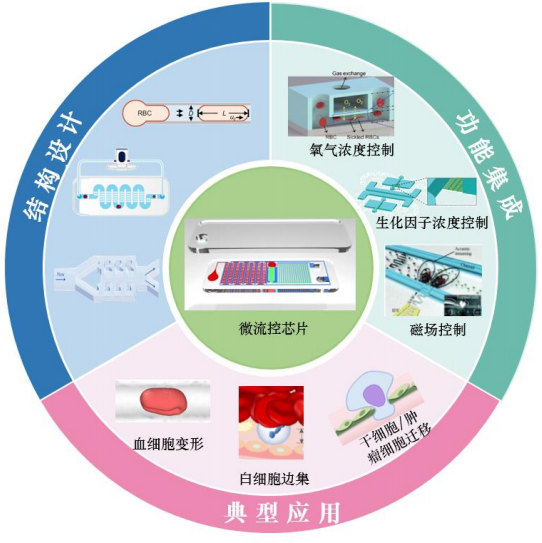
圖 1 不同結構設計的微流控芯片系統在細胞力學研究領域的應用概述
1 微流控芯片系統及數值模型模擬在紅細胞流動變形行為研究進展
1.1 基于微流控芯片系統的紅細胞變形特性研究
用于紅細胞變形性研究的微流控芯片可根據芯片復雜程度分為兩大類:單通道芯片和多通道芯片。他們可以分別用于模擬紅細胞在直通毛細血管和復雜血管分支網絡中的流動行為。單通道微流控芯片具有高靈敏度,可以直接觀察到細胞和亞細胞水平的動態過程。Quinn 等人通過單通道微流控芯片定量探究了健康紅細胞在毛細血管內的流變規律。他們通過調節通道出入口的壓力差控制流體流速,以模擬真實毛細血管中的流動工況。在壓力驅動下,紅細胞可以穿過橫截面積只有 8 平方微米左右的狹窄通道,發現細胞流動速度與壓力差存在線性關系。鑒于紅細胞流變學功能障礙的一個常見指標是紅細胞可變形性的降低,探究紅細胞的變形能力對于理解相關血液疾病具有重要意義。基于此,Guo 等人在此芯片基礎上進行了改進,設計了多個串行的漏斗形漸縮毛細通道來探究健康紅細胞的擠壓變形規律。他們發現了一個具有高度可重復性的物理量——皮質張力來表征紅細胞的變形性能。類似地,皮質張力可用于衡量病理條件下紅細胞的變形性能,輔助相關血液疾病(如遺傳性球形紅細胞癥、鐮狀紅細胞貧血癥等)的臨床診斷,從而獲得有關血液疾病臨床狀態以及藥物治療的一些關鍵信息。Guo 等人將這樣的微流控芯片用于研究瘧疾感染紅細胞的變形性能的變化,并根據測定的紅細胞過毛細通道的驅動壓力值來判斷惡性瘧原蟲感染紅細胞的嚴重程度。
由于單通道微流控芯片的通量有限,無法并行研究多個細胞的力學表型,人們設計出了多通道微流控芯片來彌補單通道芯片的通量缺陷,以滿足瘧疾患者血樣中的低濃度瘧疾感染紅細胞的收集和分析。此外,多通道微流控芯片的多維網格可以模擬復雜的分支血管形態,構建更逼真的血流微循環環境。Bow 等人設計了一種多通道并行排列的微管道陣列,利用寬度僅為 3 微米的通道構建受限空間。在這樣的微流控芯片中,健康的紅細胞會快速通過微通道,而瘧疾感染紅細胞因其較差的變形性而難以擠入狹窄微通道。鐮狀紅細胞貧血癥是一種常見的遺傳性血液疾病,臨床表現為慢性溶血性貧血、易感染和再發性疼痛危象以及局部缺血,導致組織器官損害。由于鐮變紅細胞對微環境中的氧氣濃度十分敏感,想要模擬紅細胞在毛細血管中的流動及堵塞需要實驗裝置能實現對氧氣濃度的調控,這對常規實驗裝置來說是個極大的挑戰。Du 等人利用互聯多通道微流控裝置解決了這一難題,并實現了氧氣濃度可調的仿生毛細血管微環境。通過調節氧氣濃度,可以控制紅細胞的鐮變過程并分析紅細胞從發生鐮變到導致鐮狀細胞危象的整個過程。鐮變紅細胞不僅影響自身變形能力造成毛細血管及小靜脈堵塞,還會增加血液粘滯性,從而導致一系列炎癥反應并在相應部位產生疼痛危象。Papageorgiou 等人通過微流控實驗發現鐮變初期的紅細胞在毛細管中顯著地粘附于管道內壁,低氧濃度會進一步增強鐮變紅細胞的粘附,但氧氣濃度的改變對鐮變末期的紅細胞的粘附能力無明顯影響。
1.2 基于微流控芯片系統的紅細胞疲勞特性研究
紅細胞隨血流在體內流動時,當流經毛細血管時會發生擠壓變形,其形態從雙凹圓盤形逐漸轉變為球形,變形性下降,進而造成毛細血管的堵塞。另外,在血液儲存過程中,紅細胞的形態、結構和功能也會發生變化,這些變化被稱為儲存損傷。近年來,一些學者采用微流控實驗方法從形態學、生物力學等角度對紅細胞儲存損傷展開研究,例如,Zheng 等基于雙流體聚焦原理,采用微流控實驗方法研究了紅細胞在儲存周期內變形性的改變。研究發現,隨著儲存時間增加,球形紅細胞數目增多,紅細胞的分布寬度也會明顯變寬。但紅細胞的松弛時間恢復系數卻顯著降低,證實是由于紅細胞內 ATP 的消耗引發細胞骨架重組,導致細胞膜硬化和更快的恢復速率。這些結果表明可以使用時間恢復系數和細胞分布寬度來衡量儲存的紅細胞質量。
紅細胞疲勞是指在機械拉伸力的循環加載下,其形態和力學特性呈現顯著變化的現象。然而,紅細胞在體內循環時受到擠壓變形而導致的疲勞損傷程度很難在體內直接測量,這給研究疲勞過程中紅細胞的變形特性和生物力學特性帶來了巨大挑戰。近年來,研究人員借助微流控平臺嘗試在體外模擬這一過程,以研究紅細胞疲勞的潛在影響機制。例如,Sakuma 等人采用微流控實驗方法(如圖 2),提出了一種衡量紅細胞疲勞狀態的指標。他們通過注射器對微通道中的紅細胞傳遞往復的機械應力,精準控制紅細胞數百次的循環擠壓變形。研究發現,隨著循環擠壓次數的增加,紅細胞逐漸失去變形能力:微通道出口處的細胞長度與細胞離開通道后的長度相等,并且不同細胞樣本具有相同的疲勞趨勢和不同的臨界數值。這些結果證實了采用細胞失去變形能力的臨界擠壓數值來評價疲勞狀態的可行性。進一步研究發現該臨界數值與變形指數呈線性關系,因此變形指數也可作為細胞疲勞狀態的評價指標。Qiang 等人采用調幅電變形和微流控芯片系統來表征單個紅細胞的動態疲勞程度。該方法不僅可以對通道內的紅細胞施加靜態載荷,也可以通過在微流控裝置的交叉電極兩端加載正弦波信號,實現紅細胞的循環拉伸變形。研究發現隨著拉伸次數增加,紅細胞逐漸喪失可恢復性,且峰值載荷越大,細胞變形能力下降更加顯著。該結果證實了在循環載荷作用下,紅細胞也會產生機械疲勞效應,且在相同的累積加載時間和相同的最大載荷下,循環載荷對紅細胞造成的膜損傷明顯大于持續的靜態載荷情況。此外,Pan 等人設計了類似 ECMO 結構的多通道微流控芯片,研究了紅細胞在周期性擠壓下的疲勞響應機制。他們發現,當紅細胞經歷周期性擠壓變形后,細胞內 ATP 水平降低,其形態逐漸棘形化,導致變形能力下降;然而,在低擠壓頻率下,細胞不容易出現機械疲勞現象。這些結果揭示了以擠壓頻率為主導的疲勞機制,并表明細胞疲勞程度與細胞內 ATP 水平的關聯性。由此可見,機械疲勞在影響細胞力學特性方面有著重要作用。
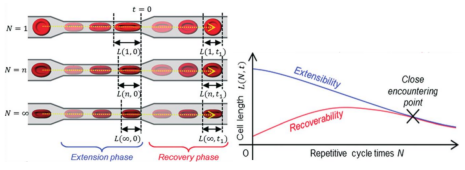
圖 2 采用微流控芯片技術評估紅細胞的疲勞損傷程度
紅細胞在其生命周期內會不斷經歷循環擠壓變形,直至被脾臟清除。為了更好地了解脾臟清除衰老紅細胞的潛在力學機制,Antoni 等人設計了一種含有狹窄微通道的微流控芯片,用來研究紅細胞在循環應力作用下反復穿越脾狹縫的流動變形特性。他們通過量化紅細胞擠壓次數與細胞體積、球度指數、彎曲模量等參數的變化關系,并結合細胞骨架-膜蛋白成分分析,認為囊泡的釋放、細胞球形化及膜蛋白損失是導致衰老紅細胞更易被巨噬細胞吞噬清除的主要原因。此外,在血液循環中,紅細胞會反復流經富陽和缺氧的器官組織,氧張力水平的反復變化會影響血紅蛋白的氧親和力,從而改變細胞的變形性能。例如,在鐮狀紅細胞貧血病中,研究表明氧氣轉運機制障礙會導致紅細胞變形能力下降。為此,Qiang 等人采用微流控芯片系統分析了缺氧環境對紅細胞疲勞特性的影響。基于不同低氧濃度環境的實驗結果,他們分析了健康紅細胞和鐮狀紅細胞經歷不同拉伸時間后的變形性能變化,發現鐮狀紅細胞會更快進入疲勞狀態。
1.3 紅細胞在微管道中流動變形的數值模型模擬
人們通過設計不同的微流控芯片系統對紅細胞的流動變形特性進行了大量的實驗研究。然而,關于單個紅細胞在最小毛細管相關長度尺度(約3 微米)中的流動特性僅有定性結果,缺乏充足的定量分析來更好地理解紅細胞的流動變形規律及影響機制。此外,微流控通道只能觀測到紅細胞的二維變化,第三個維度上的數據無法通過實驗直接獲取。因此,學者們基于微流控實驗結果建立了紅細胞的數值模型,模擬生理/病理紅細胞在穿越脾臟內皮間狹縫、毛細血管、復雜血管分支網絡等多個尺度管道時的不同流變學特性(見圖 3(1))。
脾臟在人體中起著儲存血液、造血、清除老化紅細胞和進行免疫應答的角色,其清除老化血細胞的力學機制就是利用狹窄的內皮間狹縫過濾變形性能較差的病變或衰老紅細胞。Pivkin 等人通過數值模擬發現紅細胞的體面比比其膜剛度更能決定紅細胞在脾狹縫中的截留率。Ma 及其合作者利用類似的數值模型發現在紅細胞達到被困在脾狹縫中的臨界體面比之前,紅細胞直徑的減小可以縮短其通過脾狹縫所需的時間,而膜粘度的增加則會減慢其通過速度(如圖 3(2))。此外,老化相關的膜面積損失過程中,需要更大的臨界壓力梯度才能使紅細胞變形以通過脾狹縫,從而導致更強烈的損傷,使得其在下一輪脾狹縫“考驗”中的截留概率升高。Quinn 等人在單通道微流控實驗基礎上進行了基于耗散粒子動力學方法的數值模擬(如圖 3(3)),表征了紅細胞在穿越寬度分別為 3 微米及 6 微米的毛細通道時的局部膜面積膨脹率,發現紅細胞的頭部面積膨脹最多,表明在變形時紅細胞頭部受到的應力最大。為了深入了解在多級血管中紅細胞的流動特性,Li 等人發展了一個具有流入/流出邊界條件的模型模擬方法,用于模擬研究紅細胞懸浮液在分叉微血管網絡中的流動變形行為。他們的結果表明,流體在微血管主分叉管道內的速度幅度較大,而在小分支內的速度幅度相對均勻,速度分布呈典型的塞狀(如圖 3(4))。Wang 等人使用浸入式邊界方法對紅細胞在不同直徑微通道內流動、變形和傳質進行了數值分析,從細胞尺度闡明了微循環系統中細胞膜的力學特性與流場剪切特性和微管對細胞的幾何約束等多種因素之間相互耦合作用下的傳質特性。Ai 等人利用浸沒有限元方法研究了零質量射流作用下紅細胞在微通道中的運動變形過程, 分析了壓力梯度和射流振動頻率、振幅等參數對細胞膜力敏通道開啟程度的影響規律。Xiao 等人借助耗散粒子動力學模擬方法研究了紅細胞在漸縮-漸擴通道內的流動變形行為,分析了頸縮口尺寸等因素對紅細胞通過漸縮-漸擴通道的影響規律。Ye 等人利用耗散粒子動力學及光滑粒子流體動力學模擬方法研究了紅細胞在復雜管內及流體芯片中的運動、變形以及聚集行為。這些模擬研究可幫助人們在細胞-亞細胞等層面理解健康和血液疾病中的紅細胞在毛細血管內的流動規律及機制。
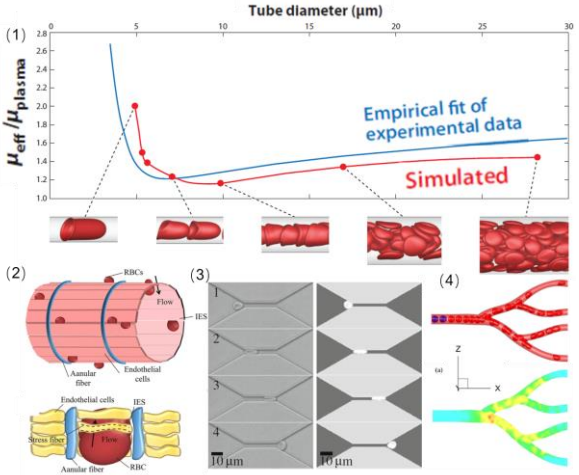
圖 3 紅細胞在微管道中流動變形的數值模擬
(1)不同尺度下紅細胞變形及粘滯阻力的模擬及實驗結果;(2)脾狹縫的微結構;(3)紅細胞在仿生毛細血管中的流動變形;(4)紅細胞在仿生分叉微血管中的流動變形及分布特征。
免責聲明:文章來源力學學報 以傳播知識、有益學習和研究為宗旨。 轉載僅供參考學習及傳遞有用信息,版權歸原作者所有,如侵犯權益,請聯系刪除。
標簽: 微流控芯片