開發(fā)一種基于納米微流控芯片的胰腺癌外泌體的特異性檢測方法
2021年1月6日,韓國中央大學(xué)Jonghoon Choi教授團(tuán)隊(duì)和東國大學(xué)Kyobum Kmin教授團(tuán)隊(duì)合作, 在Biosens Bilelectron 在線發(fā)表題為“exosome-mediated diagnosis of pancreatic cancer using lectinconjugated nanoparticles bound to selective glycans”的研究成果。研究利用胰腺癌細(xì)胞來源的外泌體膜表面富含特異性聚糖成分、且可與特定凝集素結(jié)合的特點(diǎn),設(shè)計(jì)開發(fā)可同時結(jié)合特定凝集素和微流控芯片的聚苯乙烯納米粒子,通過檢測被微流控芯片捕獲的納米粒子上的結(jié)合的凝集素?zé)晒庑盘枏?qiáng)度,定量分析外周血中胰腺癌來源外泌體的含量。這種高度特意、敏感的胰腺癌來源外泌體的檢測方法的開發(fā),為實(shí)現(xiàn)胰腺癌早期診斷提供了有力的液體活檢工具。
胰腺癌尚缺乏有效的早期診斷方法,外泌體因其在循環(huán)系統(tǒng)中的穩(wěn)定性和聚集特征,作為新興標(biāo)志物備受矚目。在正常細(xì)胞轉(zhuǎn)變?yōu)槟[瘤細(xì)胞的過程中,細(xì)胞膜蛋白、脂質(zhì)和胞質(zhì)蛋白通過轉(zhuǎn)錄后修飾發(fā)生糖基化。糖基化參與調(diào)節(jié)細(xì)胞狀態(tài)、生理功能和病理生理過程,腫瘤中糖基化被認(rèn)為是預(yù)測癌癥預(yù)后的膜成分,因此外泌體聚糖成分可以作為癌癥檢測的標(biāo)志物。然而,利用外泌體作為剩余標(biāo)志物存在很多障礙,例如分離外泌體存在的困難,以及難以區(qū)分正常或疾病相關(guān)外泌體。常規(guī)外泌體檢測技術(shù)利用抗體選擇性檢測疾病特異性標(biāo)志物,盡管這一方法已被廣泛應(yīng)用,但由于癌細(xì)胞的異質(zhì)性及其導(dǎo)致腫瘤相關(guān)遺傳信息和蛋白質(zhì)的變化,常規(guī)方法診斷準(zhǔn)確性可能會受到影響。
利用多糖特異性成分靶向癌癥來源外泌體的方法能夠有效的克服目前癌癥診斷和檢測的困境。凝集素是一種聚糖連接蛋白,能夠特異性靶向腫瘤細(xì)胞的聚糖成分,有助于在臨床診斷中的應(yīng)用。研究報(bào)道使用凝集素來量化癌癥患者血清中特定的糖基化蛋白,根據(jù)凝集素與聚糖結(jié)合的親和力可開發(fā)一種簡便的、具有選擇性的外泌體捕獲方法。此外,與用于癌癥診斷的常規(guī)生物分子檢測不同,使用凝集素-聚糖互相作用可避免來自血液中蛋白質(zhì)和肽或變性標(biāo)志物的非特異性競爭。
因此,利用微流控芯片中的雙功能納米顆粒實(shí)現(xiàn)了基于凝集素的外泌體檢測。以聚苯乙烯納米粒子為原料,通過在納米粒子的一半表面沉積金的方法制備了雙功能納米粒子janus 納米粒子(JNP)。JNP包括兩個部分:一個用于將凝集素結(jié)合在聚苯乙烯表面,另一個用于在EXO芯片的固定粒子。
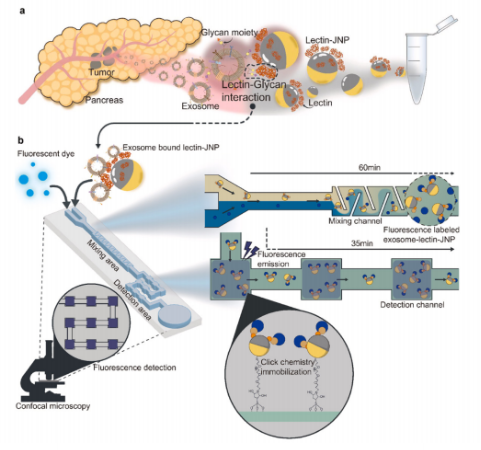
圖1 凝集素-JNP檢測胰腺癌外泌體
研究團(tuán)隊(duì)驗(yàn)證,從兩個胰腺癌細(xì)胞系和患者血漿樣本中獲得的胰腺癌細(xì)胞來源的外泌體,成功地被凝集素結(jié)合的JNP捕獲,其親和力與CA19-9(一種常規(guī)抗體)相當(dāng)。此外,利用該平臺檢測外泌體可以區(qū)分轉(zhuǎn)移性和非轉(zhuǎn)移性的多糖特性,為開發(fā)新的早期診斷標(biāo)志物提供了可能。
免責(zé)聲明:文章來源網(wǎng)絡(luò) 以傳播知識、有益學(xué)習(xí)和研究為宗旨。 轉(zhuǎn)載僅供參考學(xué)習(xí)及傳遞有用信息,版權(quán)歸原作者所有,如侵犯權(quán)益,請聯(lián)系刪除。
標(biāo)簽: 微流控芯片